বোরের মডেলে যে শক্তিস্তরের কথা বলা হয়েছে তাকে প্রধান শক্তিস্তর বলা হয়। প্রতিটি প্রধান শক্তিস্তরের সর্বোচ্চ ইলেকট্রন ধারণ ক্ষমতা 2n2 যেখানে n = 1, 2, 3, ……… ইত্যাদি।
অতএব, সূত্রানুসারে-
K শক্তিস্তরের জন্য n = 1,
অতএব, K শক্তিস্তরের সর্বোচ্চ ইলেকট্রন থাকতে পারে 2n2 = (2×12) টি = 2 টি।
L শক্তিস্তরের জন্য n = 2,
অতএব, L শক্তিস্তরের সর্বোচ্চ ইলেকট্রন থাকতে পারে 2n2 = (2×22) টি = 8 টি।
M শক্তিস্তরের জন্য n = 3,
অতএব, M শক্তিস্তরের সর্বোচ্চ ইলেকট্রন থাকতে পারে 2n2 = (2×32) টি = 18 টি।
N শক্তিস্তরের জন্য n = 4,
অতএব, N শক্তিস্তরের সর্বোচ্চ ইলেকট্রন থাকতে পারে 2n2 = (2×42) টি = 32 টি।
মৌলের ইলেকট্রন বিন্যাস [H(1) থেকে Zn(30) পর্যন্ত]
| পারমাণবিক সংখ্যা | মৌল | K | L | M | N |
| 1 | H | 1 | |||
| 2 | He | 2 | |||
| 3 | Li | 2 | 1 | ||
| 4 | Be | 2 | 2 | ||
| 5 | B | 2 | 3 | ||
| 6 | C | 2 | 4 | ||
| 7 | N | 2 | 5 | ||
| 8 | O | 2 | 6 | ||
| 9 | F | 2 | 7 | ||
| 10 | Ne | 2 | 8 | ||
| 11 | Na | 2 | 8 | 1 | |
| 12 | Mg | 2 | 8 | 2 | |
| 13 | Al | 2 | 8 | 3 | |
| 14 | Si | 2 | 8 | 4 | |
| 15 | P | 2 | 8 | 5 | |
| 16 | S | 2 | 8 | 6 | |
| 17 | Cl | 2 | 8 | 7 | |
| 18 | Ar | 2 | 8 | 8 | |
| 19 | K | 2 | 8 | 8 | 1 |
| 20 | Ca | 2 | 8 | 8 | 2 |
| 21 | Sc | 2 | 8 | 9 | 2 |
| 22 | Ti | 2 | 8 | 10 | 2 |
| 23 | V | 2 | 8 | 11 | 2 |
| 24 | Cr | 2 | 8 | 13 | 1 |
| 25 | Mn | 2 | 8 | 13 | 2 |
| 26 | Fe | 2 | 8 | 14 | 2 |
| 27 | Co | 2 | 8 | 15 | 2 |
| 28 | Ni | 2 | 8 | 16 | 2 |
| 29 | Cu | 2 | 8 | 18 | 1 |
| 30 | Zn | 2 | 8 | 18 | 2 |
হাইড্রোজেনের (H) পারমাণবিক সংখ্যা 1। ফলে এর ইলেকট্রন সংখ্যাও 1। তাই একটি ইলেকট্রন প্রথম শক্তিস্তর K-তে প্রবেশ করবে।
হিলিয়ামের (He) পারমাণবিক সংখ্যা 2. অতএব ইলেকট্রন দুটি প্রথম শক্তিস্তর K-তে প্রবেশ করবে।
লিথিয়ামের (Li) পারমাণবিক সংখ্যা 3. ফলে প্রথম শক্তিস্তর K-তে 2 টি ইলেকট্রন প্রবেশ করবে।
যেহেতু K প্রধান শক্তিস্তরে দুটির বেশি ইলেকট্রন থাকতে পারে না তাই এর তৃতীয় ইলেকট্রনটি দ্বিতীয় শক্তিস্তর L তে প্রবেশ করবে।
আবার, সোডিয়ামের (Na) এর পারমাণবিক সংখ্যা 11. তাই K শক্তিস্তরে 2 টি, L প্রধান শক্তিস্তরে 8 টি বাকি 1 টি ইলেকট্রন M শক্তিস্তরে প্রবেশ করবে।
ইলেকট্রন বিন্যাস ভালোভাবে খেয়াল করলে দেখতে পাবে হাইড্রোজেন (H) থেকে আর্গন (Ar) পর্যন্ত উপরে যে নিয়ম বর্ণনা করা হয়েছে সেই নিয়মেই ইলেকট্রন বিন্যাস হয়েছে। কিন্তু নিয়মটির ব্যতিক্রম ঘটেছে পটাশিয়াম (K) থেকে পরবর্তী মৌলগুলোতে। কেননা, আমরা জানি তৃতীয় শক্তিস্তর (M) এর সর্বোচ্চ ইলেকট্রন ধারণ ক্ষমতা 18 টি। কিন্তু পটাশিয়ামের 19 তম ইলেকট্রন এবং ক্যালসিয়ামের (Ca) 19 তম ও 20 তম ইলেকট্রন তৃতীয় শক্তিস্তর (M) কে অপূর্ণ রেখে আগেই চতুর্থ (N) শক্তিস্তরে প্রবেশ করে।
স্ক্যানডিয়ামের (Sc) ক্ষেত্রে 19তম ও 20তম ইলেকট্রন চতুর্থ শক্তিস্তরে যাবার পর 21তম ইলেকট্রনটি আবার তৃতীয় শক্তিস্তরে প্রবেশ করেছে।
পারমাণবিক সংখ্যা 19 থেকে পরবর্তী মৌলগুলোতে আগে চতুর্থ প্রধান শক্তিস্তরে (N) দুটি ইলেকট্রন পূরণ করে তারপর ইলেকট্রন তৃতীয় প্রধান শক্তিস্তর M এ প্রবেশ করে। এরপরও Cr ও এর ইলেকট্রন বিন্যাসে বিশেষ ব্যতিক্রম লক্ষ করা যাচ্ছে। এই বিষয়টি বোঝার জন্য আমাদের উপশক্তিস্তরের ধারণাটি থাকতে পারে।
উপশক্তিস্তরের ধারণা
প্রতিটি প্রধান শক্তিস্তর n দিয়ে চিহ্নিত করা হয়। এই শক্তিস্তরগুলো আবার উপশক্তিস্তরে বিভক্ত থাকে এবং এই উপশক্তিস্তরকে 1 দ্বারা চিহ্নিত করা হয়। 1 এর মান হয় 0 থেকে n-1 পর্যন্ত। উপশক্তিস্তরগুলোকে অরবিটাল বলা হয়। এই উপশক্তিস্তর বা অরবিটালগুলোকে s, p, d, f ইত্যাদি নামে আখ্যায়িত করা হয়। বিভিন্ন উপশক্তিস্তরের জন্য সম্ভাব্য 1 এর মান নিচে দেখানো হলোঃ
n = 1 হলে l = 0 অরবিটাল একটি: 1s
n = 2 হলে l = 0, 1 অরবিটাল দুইটি: 2s, 2p
n = 3 হলে l = 0, 1, 2 অরবিটাল তিনটি: 3s, 3p, 3d
n = 4 হলে l = 0, 1, 2, 3 অরবিটাল চারটি: 4s, 4p, 4d, 4f
n = 5 হলে l = 0, 1, 2, 3, 4 অর্থাৎ এখানে অরবিটাল থাকবে পাঁচটি কিন্তু 4s, 4p, 4d, 4f এই প্রথম চারটি অরবিটালেই সবগুলো ইলেকট্রনের বিন্যাস করা সম্ভব বলে পরবর্তী অরবিটালের আর প্রয়োজন হয় না। n = 6, 7 এবং 8 এর জন্যেও এটি সত্যি।
প্রতিটি অরবিটালে ইলেকট্রন সংখ্যা হচ্ছে: 2(2l+1)
প্রতিটি পূর্ণ শক্তিস্তরে ইলেকট্রনের সংখ্যা হচ্ছে 2n2 এবং সবগুলো অরবিটালের ইলেকট্রনের সংখ্যা যোগ করে পাওয়া যায় 2n2।
শক্তিস্তরে ইলেকট্রন বিন্যাস (n = 1 থেকে 4 পর্যন্ত)
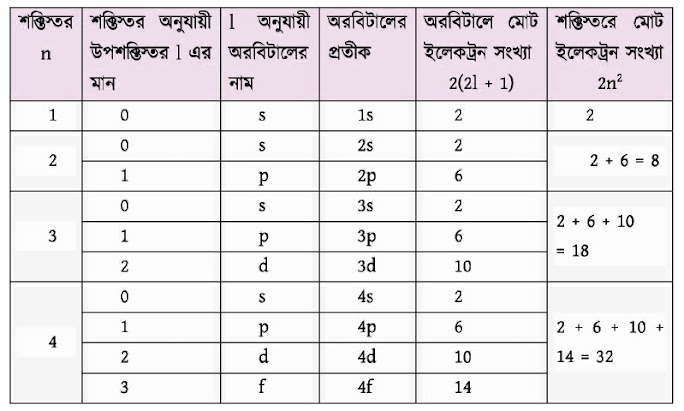
পরমাণুতে ইলেকট্রন বিন্যাসের নীতি
পরমাণুতে ইলেকট্রন প্রথমে সর্বনিম্ন শক্তির অরবিটালে প্রবেশ করে এবং পরে ক্রমান্বয়ে উচ্চ শক্তির অরবিটালে প্রবেশ করে। অর্থাৎ যে অরবিটালের শক্তি কম সেই অরবিটালে ইলেকট্রন আগে প্রবেশ করবে এবং যে অরবিটালের শক্তি বেশি সেই অরবিটালে ইলেকট্রন পরে প্রবেশ করবে।
অরবিটালের মধ্যে কোনটির শক্তি কম আর কোনটির শক্তি বেশি তা অরবিটাল দুটির প্রধান শক্তিস্তরের মান (n) এবং উপশক্তিস্তরের মান (l) এর যোগফলের উপর নির্ভর করে।
যে অরবিটালের (n+l) এর মান কম সেই অরবিটালের শক্তি কম এবং সেই অরবিটালেই ইলেকট্রন আগে প্রবেশ করবে।
অপরদিকে, (n+l) এর মান যে অরবিটালের বেশি তার শক্তিও বেশি এবং সেই অরবিটালেই ইলেকট্রন পরে প্রবেশ করবে।
3d অরবিটালের জন্য n=3 এবং l = 2।
অতএব, (n+l) এর মান (3+2)=5
আবার, 4s অরবিটালের জন্য n=4, l=0
অতএব, n+l এর মান 4+0 = 4
কাজেই 3d অরবিটালের চেয়ে 4s অরবিটাল কম শক্তি সম্পন্ন। তাই ইলেকট্রন প্রথমে 4s অরবিটালে এবং পরে 3d অরবিটালে প্রবেশ করবে।
আবার, দুটি অরবিটালের (n+l) এর মান যদি সমান হয় তাহলে যে অরবিটালটিতে n এর মান কম সেই অরবিটালে শক্তি কম হবে এবং সেই অরবিটালে ইলেকট্রন আগে প্রবেশ করবে।
অপরদিকে, সমান (n+1) এর মানের জন্য যে অরবিটালের n এর মান বেশি, সেই অরবিটালের শক্তিও বেশি, কাজেই সে অরবিটালে ইলেকট্রন পরে প্রবেশ করবে।
যেমন – 3d ও 4p এর (n+l) এর মান যথাক্রমে 3+2 = 5 এবং 4 + 1 = 5 কিন্তু যেহেতু 3d অরবিটারে n এর মান কম, তাই এ অরবিটালের শক্তি কম এবং এ অরবিটালে ইলেকট্রন আগে প্রবেশ করবে।
অপরদিকে, 4p অরবিটালে n অরবিটালে n এর মান বেশি হওয়ায় এর শক্তি 3d এর চেয়ে বেশি। তাই এ অরবিটালে ইলেকট্রন পরে প্রবেশ করবে।
এ হিসাব অনুযায়ী পরমাণুর অরবিটালের ক্রমবর্ধমান শক্তি হবে এরকমঃ

উপস্তরগুলোর শক্তির ক্রমগুলো মনে রাখার জন্য নিচের ছকটির সাহায্য নেওয়া যায়ঃ
দেখা যাচ্ছে, s উপশক্তিস্তরে সর্বোচ্চ 2 টি ইলেকট্রন, p উপশক্তিস্তরে সর্বোচ্চ 6 টি ইলেকট্রন, d উপশক্তিস্তরে সর্বোচ্চ 10 টি ইলেকট্রন এবং f উপশক্তিস্তরে সর্বোচ্চ 14 টি ইলেকট্রন থাকতে পারে।
এই নীতি অনুসারে আমরা নিম্নের মৌলগুলোর ইলেকট্রন বিন্যাস বিশ্লেষণ করতে পারব।

যেহেতু 4s অরবিটালের শক্তি 3d অরবিটালের শক্তির চেয়ে কম, তাই পটাশিয়ামের সর্বশেষ 19তম ইলেকট্রনটি 3d অরবিটালে প্রবেশ না করে 4s অরবিটালে প্রবেশ করে।
আবার, স্ক্যান্ডিয়ামের ক্ষেত্রে 19 ও 20তম ইলেকট্রন অরবিটাল পূর্ণ করে পরবর্তী উচ্চ শক্তি সম্পন্ন অরবিটালে (3d) সর্বশেষ বা 21তম ইলেকট্রন প্রবেশ করে।
বিশেষ করে মনে রাখতে হবে যে যখন ইলেকট্রন বিন্যাস লিখতে হবে তখন একই প্রধান শক্তিস্তরের সকল উপশক্তিস্তর পাশাপাশি লিখতে হবে। তা না হলে ইলেকট্রনের বিন্যাস লিখার সময় ভুল হয়ে যেতে পারে।

ইলেকট্রন বিন্যাসের সাধারণ নিয়মের কিছু ব্যতিক্রম
সাধারণভাবে দেখা যায় যে, একই উপশক্তিস্তর p ও d এর অরবিটালগুলো অর্ধেক পূর্ণ (p3, d5) বা সম্পূর্ণরূপে পূর্ণ (p3, d10) হলে সে ইলেকট্রন বিন্যাসে সুস্থিত হয়। তাই Cr(24) এর ইলেকট্রন বিন্যাস স্বাভাবিকভাবে হওয়ার কথাঃ
Cr(24)=1s22s22p63s23p63d44s2 কিন্তু 3d অরবিটাল সুস্থিত অর্ধপূর্ণ হওয়ার আকাঙ্ক্ষায় 4s অরবিটাল হতে একটি ইলেকট্রন 3d অরবিটালে আসে। ফলে ক্রোমিয়ামের ইলেকট্রন বিন্যাস হয় এরকমঃ
Cr(24)=1s22s22p63s23p63d54s1